如何通过化学考试
作者:
Roger Morrison
创建日期:
3 九月 2021
更新日期:
1 七月 2024

内容
在本文中:养成良好的学习习惯理解原子结构预测化学反应在化学中应用数学使用化学语言
要在常规化学课程中取得成功,您必须了解本学科的基础知识,能够进行简单的计算,使用计算器执行更复杂的操作并准备学习真正不同的东西。化学是一门研究物质及其性质的科学。我们周围的一切都与化学有关,甚至是您可能认为很自然的最基本的事物,例如您喝的水和呼吸的空气特性。在了解您周围的世界时,即使是在原子层面上,也要对新知识保持开放。您与化学的第一次接触可能充满挑战并且令人兴奋。
阶段
第一部分:养成良好的学习习惯
-

学会认识你的老师。 要在化学课上取得成功并在课堂上取得更高的成绩,请花时间与您的老师见面并与他分享您不了解的知识。- 许多老师有学习指南,并愿意在需要的时间以外的时间接待学习者。
-

组建或加入学习小组。 如果您发现化学课程非常复杂,请不要感到羞耻。对于几乎每个人来说,这都是一个难题。- 如果您加入小组,某些成员可能会发现课程的某些部分比其他成员容易,并且可以与所有人分享他们的学习方法。划分任务。
-

阅读各章。 化学教科书并不总是最令人兴奋的书。但是,您必须花时间阅读已获得的经典著作,并突出显示您不了解的部分。尝试列出您不理解的问题或概念。- 请稍后再试以重新阅读这些难以理解的部分。如果您仍然不理解它们,请与您的学习小组,您的老师或您的助理教授进行讨论。
-

回答调查问题。 即使您对所学习的所有文档感到不知所措,也要知道您所记住的概念可能比您想像的要多。在本章末尾回答问题。- 大多数教科书提供有关如何找到正确答案的其他信息。这将使您看到推理中遗漏的内容。
-

检查图表,图片和表格。 您经常会在教科书中看到视觉效果,这将有助于您更好地理解要记住的关键元素。- 仔细查看随附的图片和标题。这可以帮助您理解一些概念。
-

寻求许可以注册课程。 很难在笔记本上记笔记,同时看板上写的东西,尤其是化学课等复杂的课程。 -

尝试使用旧的证明和旧的手册。 大多数学校都允许学习者具有参加旧考试的合法性,以帮助他们为考试做准备。- 避免简单地记住答案。在化学领域,如果您希望能够用不同的术语回答相同的问题,则必须理解这些概念。
-

查看在线帮助资源。 查看您机构化学部门提供的任何链接或在线资源。
第2部分了解原子结构
-

从最基本的结构开始。 要通过化学考试,您必须了解构成物质或质量的所有物质的基本要素。- 理解化学中最基本元素(即latome)的结构是理解该学科的第一步。课堂上将涉及的所有主题都是该基本信息的扩展。花点时间了解原子化学。
-
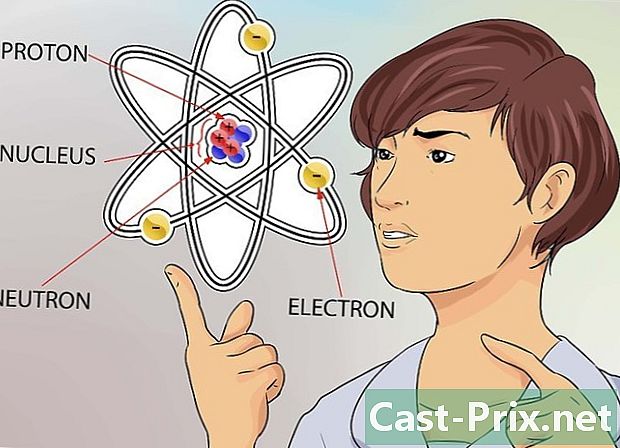
了解datome概念。 拉托姆被认为是所有物质中最小的构成元素,包括我们不能总是看到的事物,例如气体。但是,即使是很小的原子,也由构成其结构的更小的粒子组成。- 原子由中子,质子和电子组成。 latome的中心称为原子核,这个原子核由中子和质子组成。电子是引诱在latome周围的粒子,就像行星绕着太阳旋转一样。
- 原子的大小非常小,但是为了给您一个比较,请考虑一下您知道的最大的体育场。如果您将此阶段视为原子,则原子核的大小将像位于电场中心的豌豆一样大。
-
了解元素的原子结构。 这个词 元素 定义为天然物质,不能分解为其他基本元素,并且是最简单的形式。元素由硅藻组成。- 元素中存在的原子都是相同的。这意味着每个元素在其原子结构中均具有已知且唯一的中子和质子数。
-
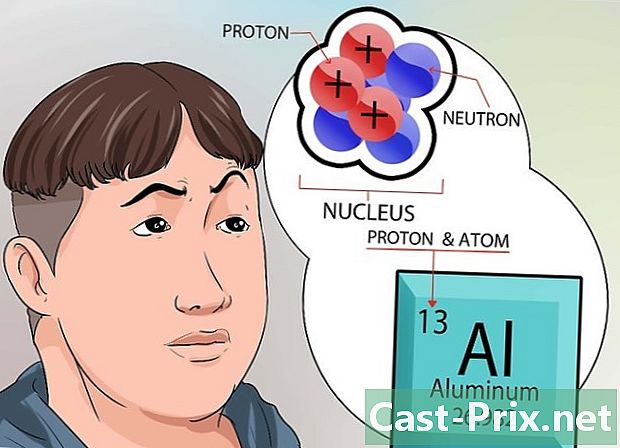
了解有关内核的更多信息。 原子核中的中子具有中性电荷。另一方面,质子带正电荷。元素的原子序数正好对应于其原子核中存在的质子数。- 您无需进行数学计算即可知道元素的质子数。该值显示在元素周期表中每个元素的每个框的顶部。
-
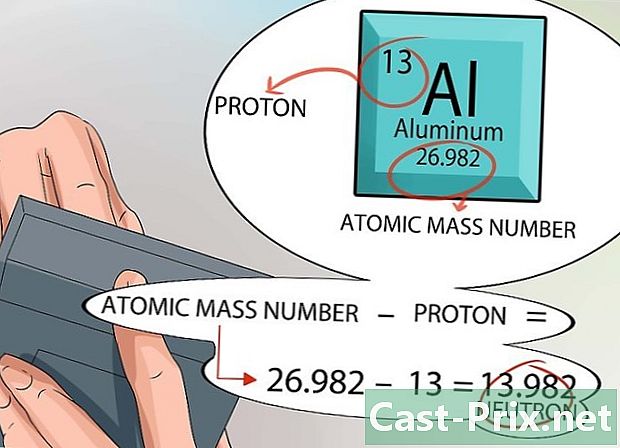
计算原子核中的中子数。 为此,您可以使用元素周期表中提供的信息。每个元素的原子数等于原子核中的质子数。- 原子质量在元素周期表的每个框中显示,并且位于元素名称下方的底部。
- 请记住,原子核中只有质子和中子。使用元素周期表,您可以知道质子的数量和化学元素的原子质量。
- 此时,计算非常简单。只需从原子质量中减去质子数即可找到该元素的拉美原子核中的中子数。
-
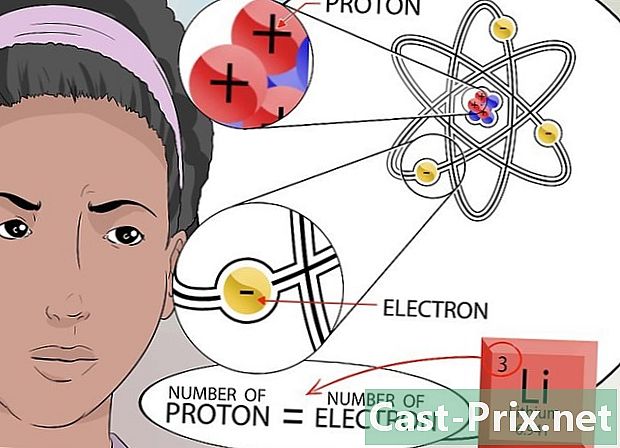
确定电子数。 请记住,相反的元素是正确的。电子是带负电荷的粒子,它们绕着原子核旋转,就像行星绕着太阳旋转一样。吸引到原子核的电子(带负电荷)的数量取决于原子核中存在的质子(带正电荷)的数量。- 由于latome的总电荷为零,因此必须平衡所有正电荷和负电荷。因此,电子的数量等于质子的数量。
-
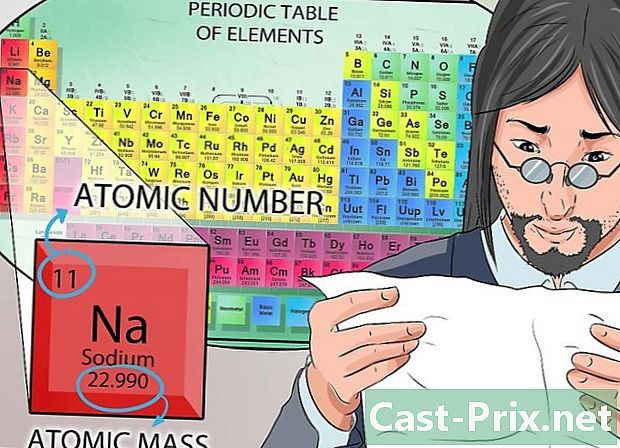
观察元素周期表。 如果您在理解化学元素的特性时遇到困难,请花点时间查看周期表上所有可用的信息。最重要的是,仔细研究图表。- 了解此图表对于化学课程第一部分的成功至关重要。
- 元素周期表仅包含元素。每两个由一个或两个符号表示。该符号唯一标识元素。例如,符号 娜 总是指钠latome。化学元素的全名通常写在符号下。
- 符号的原子序号由印刷在其上方的数字表示。原子数等于原子核中的质子数。
- 符号下的数字对应于原子质量。不要忘记这一点:原子的质量数等于原子核中所含质子和中子的总和。
-
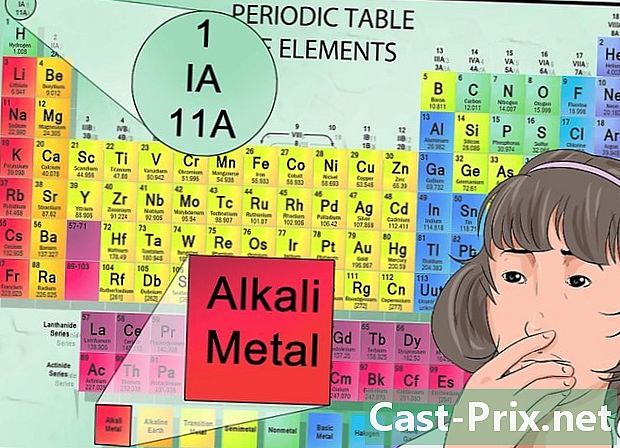
解释元素周期表。 元素周期表中有很多信息,包括每列的颜色以及元素从左到右以及从上到下的位置。
第3部分预测化学反应
-

平衡化学方程式。 在化学中,您将必须预测元素之间的反应方式。换句话说,您必须能够平衡化学反应。- 在化学方程式中,试剂位于左侧,其后是指向右侧的箭头,指示反应产物。并且方程两边的元素必须平衡。
- 例如,试剂1 +试剂2→产品1 +产品2。
- 这是锡符号的示例,锡的符号为Sn。将二氧化锡(SnO2)与气态(H2)的氢气混合。等式为SnO2 + H2→Sn + H2O。
- 然而,由于试剂的量不等于产物的量,所以该方程式是不平衡的。反应的左侧比右侧多一个氧原子。
- 使用简单的数学计算,您可以通过在左侧放置两个氢单元,在右侧放置两个水分子来平衡方程。平衡后的反应将为:SnO2 + 2 H2→Sn + 2 H2O。
-
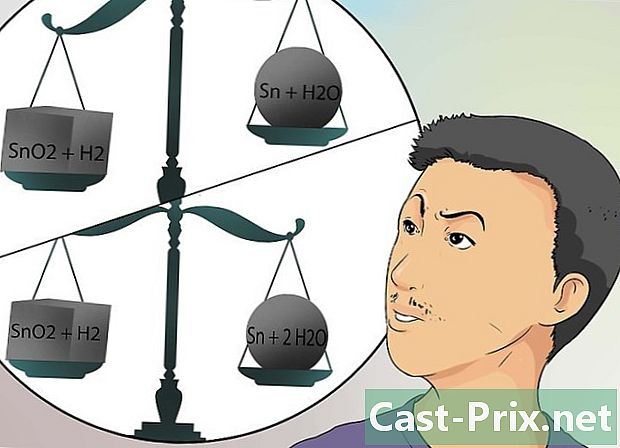
以不同的方式考虑方程式。 如果您无法平衡化学反应,请想象一下配方的哪一部分,但是您需要进行调整以或多或少地获得配方的最终产品。- 该公式为您提供了公式左侧的成分,但没有提供有关剂量的信息。但是,方程式使您知道要获得的产品价值,而总是忽略数量。您将必须找到它们。
- 始终使用上面的示例(SnO2 + H2→Sn + H2O的示例),请考虑为什么此反应(或配方公式)不起作用。等式两边的锡(Sn)量相等,氢(H2)的量相等。但是,左边有2个氧原子,右边只有1个氧原子。
- 更改方程式的右侧,以指示存在两个H2O分子(2 H2O)。前面的数字2 H2O 表示该分子的所有原子现在都加倍了。现在,氧气的数量已达到平衡,但氢气的数量却已不平衡,因为右侧的氢气比左侧的氢气更多。因此,我们必须返回方程式的左侧。修改H2成分的数量,并通过在H2前面放置系数2使其倍增。
- 在这里,您正在平衡方程式两侧的所有配料剂量。食谱中的成分与所获得的产品相同(因此是均衡的)。
-
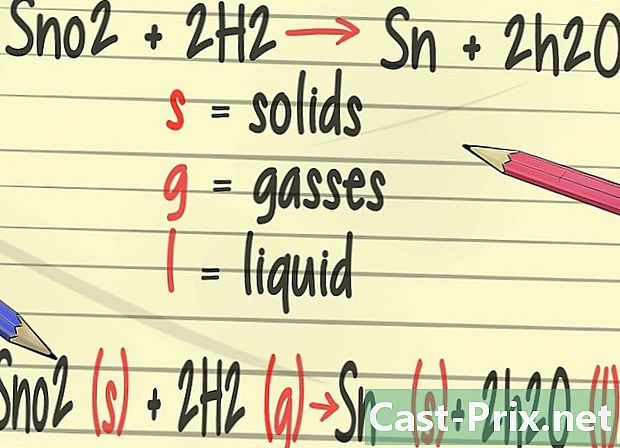
为平衡方程式添加更多细节。 在化学中,您将学习添加表示元素物理状态的符号。信 小号 代表固体,字母 g ^ 用于气体和字母 升 代表液体。 -
确定反应期间发生的变化。 化学反应首先影响基本元素或已经结合的元素,称为试剂。两种或多种试剂的组合会产生一种或多种产物。- 要通过化学考试,您必须能够求解涉及试剂,产物的方程式,并考虑其他影响其行为的因素。
-
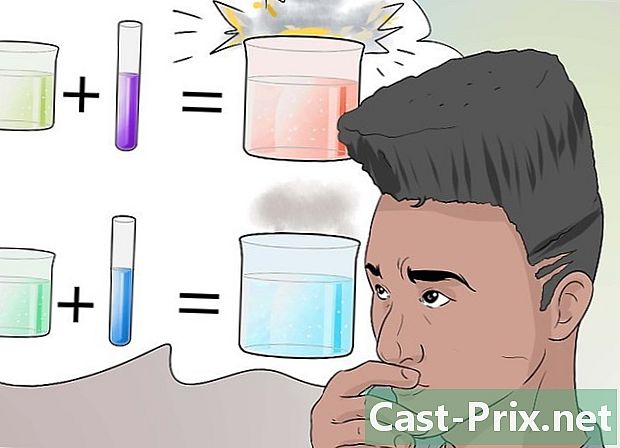
研究不同类型的反应。 发生化学反应的原因是多种因素,而不仅仅是成分的组合。- 在化学上已经研究并且您应该知道的典型反应如下:合成反应,取代,酸碱性反应,氧化还原,燃烧,水解,分解,复分解和异构化。
- 在化学课上,您的老师可能还会根据计划显示其他类型的反应。显然,高中化学课程不会像大学教授的课程那样详细。
-

使用所有可用资源。 您必须能够识别课堂上已解决的每种反馈类型的差异。使用所有学习资源,您必须了解这些概念,并在课堂上毫不犹豫地提出问题。- 反应之间的差异有时可能会使学习者感到困惑,而了解化学反应过程中发生的各种机制可能是整个课程中最复杂的部分。
-

从逻辑上理解化学反应。 不要使过程变得比现在更复杂,这会使您对通用术语感到困惑。在要研究的所有反应中,您只需要将某些东西变成其他东西。- 例如,您已经知道,通过将两个氢分子与一个氧分子结合,可以得到水。因此,如果您将水倒入锅中,然后放到火上,将会发生变化。您实际上创建了化学反应。如果将水放入冰箱,也会发生一些事情。简而言之,您引入了一个因素来改变初始试剂的状态,在我们的情况下是水。
- 逐一重写每个反应类别,直到您掌握了它,然后再转到下一个。专注于触发反应的能量来源和发生的主要变化。
- 如果您不理解这些概念,请列出所有您不了解的概念,并与您的老师,您的学习小组或一个非常擅长化学的人进行讨论。
第四部分在化学中应用数学
-

了解基本计算的顺序。 在化学中,有时需要非常详细的计算,但其他时候,基本操作就足够了。但是,必须了解确切的操作顺序才能完成并求解方程。- 记住一个缩写很简单。学生使用不同的句子来记住某些概念,数学运算的顺序也不例外。使用名称PEMDAS(源自短语Maybe My Last AS),您可以轻松记住执行数学运算的顺序。每个单词的首字母表示每个操作的顺序。首先,完成括号中的所有内容,然后是参展商,乘法,除法,加法,最后是减法。
- 按照名称PEMDAS指示的操作顺序,对该表达式3 + 2 x 2 x 6 = ___进行计算。解决方法是15。
-

了解如何舍入非常大的值。 尽管四舍五入的数字在化学中不是很常见,但有时某些复杂的数学方程式的解决方案写起来太长。仔细阅读正在进行的练习的说明,以了解是否应该对答案进行四舍五入。- 了解何时向上或向下取整。在数字序列中,如果下一位数字小于或等于4,则向下舍入。如果大于或等于5,则四舍五入到下一个数字。让我们以这个数字6为例,即66 666 666 666 666666。假设您必须弯曲到小数点后两位。答案将是6.67。
-
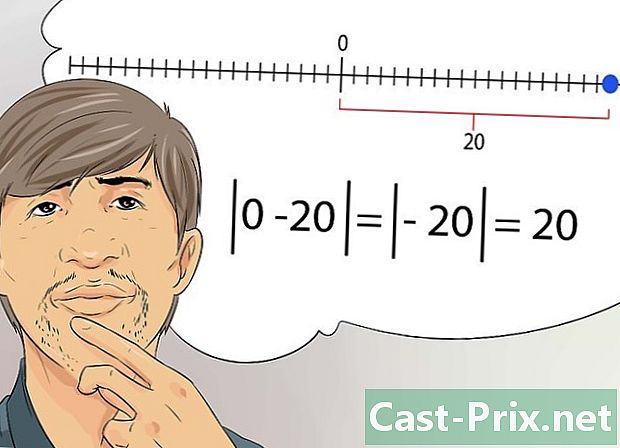
了解绝对价值的概念。 在化学中,某些数字称为绝对值,而不是实际的数学值。实数x的绝对值是该数x与零之间的距离。- 换句话说,您不再需要考虑数字的符号(正数或负数),而是要考虑其到零的距离。例如,-20的绝对值为20。
-
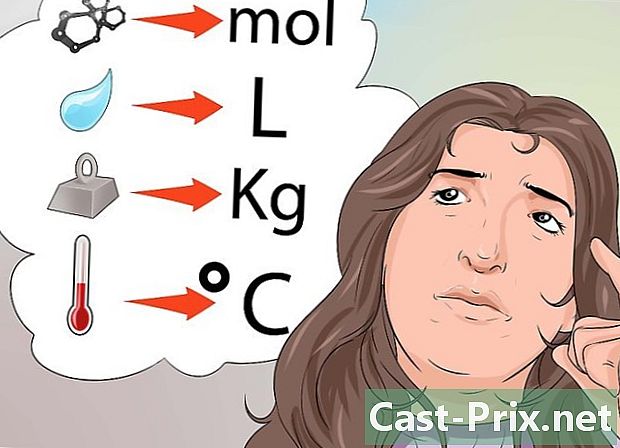
熟悉可接受的度量单位。 这里有一些例子。- 材料的量以摩尔(mol)表示。
- 温度以摄氏度(°C),华氏度(°F)或开尔文(°K)表示。
- 质量以克(g),千克(kg)或毫克(mg)表示。
- 体积和液体以升(l)或毫升(ml)表示。
-

了解如何将值从一种测量范围转换为另一种。 要通过化学考试,您将需要能够从一种公认的规模进行一些转换。例如,您可能必须从一种温度测量转换为另一种温度测量,将千克转换为磅或将升转换为液体盎司。- 有时会要求您以不同于原始单位的计量单位表达问题的解决方案。例如,假设您必须求解一个温度方程,其温度值以摄氏度为单位,但是最终答案必须以开尔文为单位。
- 开尔文(Kelvin)是化学反应中经常使用的温度测量的国际标准。练习从摄氏到开氏或华氏度。
-
花一些时间做运动。 在课堂上学习几个概念时,请花时间学习如何将度量单位从一个系统转换为另一个系统。 -

了解如何计算浓度。 加深您对百分比,比例和比率的基础知识。 -

练习营养标签。 为了通过化学考试,您应该能够轻松计算出比率,百分比,比例及其逆运算。如果您对这些概念不太了解,则需要与其他非常常见的测量单位一起训练,例如营养标签上的那些。- 检查任何食品的营养标签。您会发现每份卡路里,建议每日摄入量的百分比,总脂肪含量,脂肪中卡路里的百分比,总碳水化合物含量以及不同类型的碳水化合物的分解。了解如何从不同类别的值作为分母来计算不同的百分比。
- 例如,计算相对于产品中脂肪总量的单不饱和脂肪量。将值转换为百分比。通过使用每份的卡路里数和包装中的份数来计算产品中的卡路里数。计算一半包装产品中钠的含量。
- 通过进行此类转换的培训,无论使用什么度量单位,都可以轻松地将度量单位转换为化学量,例如摩尔/升,克/摩尔等。
-

了解如何使用Avogadro号码。 该常数表示摩尔中包含的分子,硅藻土或颗粒的数量。 Avogadro的数量是6,022 x 1023。- 例如,0.450摩尔铁中有多少个硅藻?答案是0.450 x 6022 x 1023。
-
想想胡萝卜。 如果您在化学问题上应用大量Avogadro遇到困难,请考虑使用胡萝卜而不是原子,分子或粒子。一打中有几根胡萝卜?一打有12种元素,所以一打中有12个胡萝卜。- 现在,尝试回答这个问题:痣中有多少胡萝卜?不要使用12的倍数,而要乘以Avogadro。一摩尔中有6,022 x 1,023个核心。
- 阿伏加德罗的数量用于将化学量(摩尔数)转换为许多物体(原子,分子,粒子或胡萝卜)。
- 如果您知道元素的摩尔数,则可以通过将Avogadro常数乘以所讨论的摩尔数来知道存在于此物质量中的分子,硅藻土或粒子的数目。
- 了解如何将颗粒转化为摩尔以通过化学考试非常重要。要计算比率和百分比,您需要进行摩尔换算。换句话说,您必须知道与另一单位相比以摩尔表示的元素的数量。
-
努力了解摩尔浓度的概念。 考虑溶解在液体介质中的物质的摩尔数。这是一个非常重要的示例,因为它是摩尔浓度,即以摩尔/升表示的化学物种的比例。- 在化学中,摩尔浓度用于表示液体介质中所含物质的量或液体溶液中所含溶质的量。您可以通过将溶质的摩尔数除以以升为单位的溶液体积来计算摩尔浓度。它的计量单位是每升摩尔数(mol / l)。
- 计算密度。密度也是化学中常用的度量。它表示化学物质每单位体积的质量。这里最常用的度量单位是克/升(g / l)或克/立方厘米(g / cm3)。
-

将方程式简化为经验公式。 换句话说,如果您不将方程式的最终解简化为最简单的形式,则将认为它们是错误的。- 这不适用于分子式,因为这种类型的描述表示组成分子的化学元素之间的确切比例。
-

了解分子式的概念。 您无需将分子式简化为最简单的形式或经验形式,因为它可以精确表达分子的组成。- 写一个物体的分子式就是使用化学元素的缩写以及分子中每个元素的数目datomes。
- 假设水的分子式为H2O。水的每个分子由两个氢原子和一个氧原子组成。尝试使用对乙酰氨基酚C8H9NO2的分子式进行同样的处理。实际上,所有化合物均由其分子式表示。
-

了解有关化学计量的更多信息。 您可能会满足这个学期。化学计量是使用数学公式研究化学反应的定量比例的方法。在化学计量学(应用于化学的数学)中,元素和化合物的值通常以摩尔表示,以摩尔百分比表示,以每升摩尔数或以每千克摩尔数表示。- 您将执行的最常见的数学运算之一是将克转换为摩尔。元素的原子质量单位,通常以克表示,相当于该物质的一摩尔。例如,钙latome质量为40原子质量单位。因此,40克钙等于一摩尔钙。
-

要求老师进行其他练习。 如果数学方程式和转换有问题,请与老师讨论。要求他给您更多练习来做自己,直到您清楚地了解所使用的所有概念。
第五部分使用化学语言
-
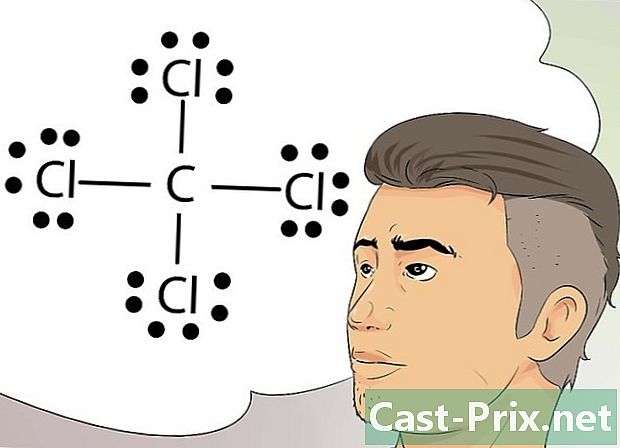
认识刘易斯的结构。 这些结构(也称为Lewis公式)是使用点表示原子外层中的成组电子和单电子的图形表示。- 这些结构对于绘制简单的图并识别原子或分子中几个元素共享的键(例如共价键)非常有用。
-

了解字节码规则。 刘易斯的结构基于此规则,该规则规定,当原子的外层恰好包含8个电子时,原子是稳定的。作为该规则的例外,氢被认为是稳定的,其外层有2个电子。 -
绘制一个Lewis结构。 这种结构由一系列点包围的元素符号表示。想象一下,它是电影的静止图像。我们没有在原子周围吸引电子,而是在给定的时间代表它们的位置。- 路易斯结构允许可视化电子的最稳定排列,即它们与另一种化学元素的连接位置。它还提供有关粘合强度的信息(例如,它们是共价键还是双键)。
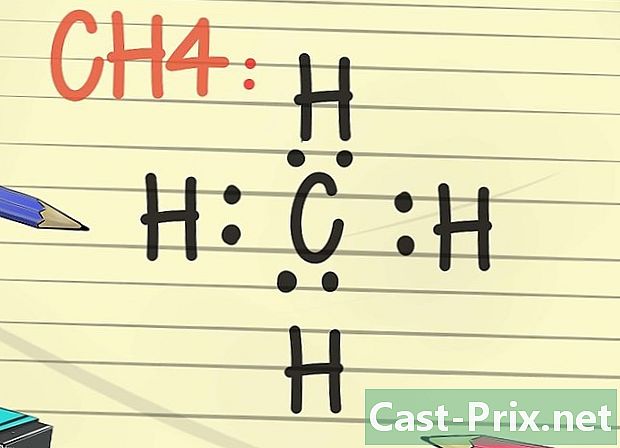
- 考虑字节规则,尝试绘制路易斯碳结构(C)。现在,在latome的每一侧(顶部,底部,左侧和右侧)放置2个点。现在,在每对点的另一侧写一个H,氢latome符号。该路易斯结构代表被四个氢原子包围的碳原子。当电子通过共价键连接时,表示碳与每个氢原子共享一个电子,这也适用于氢。
- 此示例的分子式为CH4,即甲烷。
-
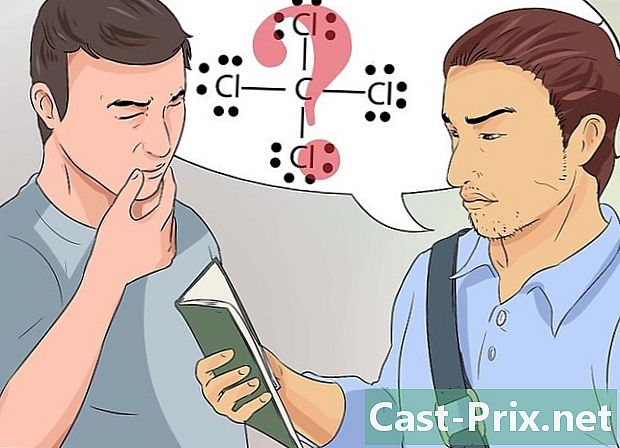
了解如何根据电子的键排列电子。 Lewis结构是化学键的简单直观表示。- 如果您不了解有关化学键和Lewis公式的某些概念,请与您的老师或研究小组讨论。
-
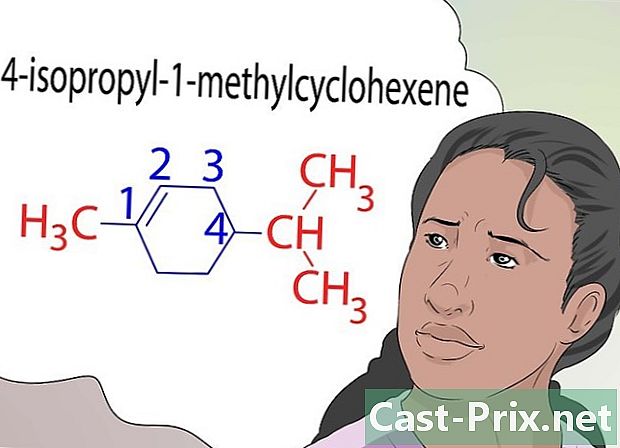
了解如何命名化合物。 化学有其关于命名法的规则。与化合物发生的反应类型,电子在外层的损失或增加以及化合物的稳定性或不稳定性是可以命名化合物的因素。 -

不要低估化学术语。 在大多数情况下,化学的第一章侧重于术语。通常,对化合物的错误识别会使您无法复查。- 如果可能,在开始课程之前,学习如何命名化合物。您可以在线购买指南或咨询资源。
-
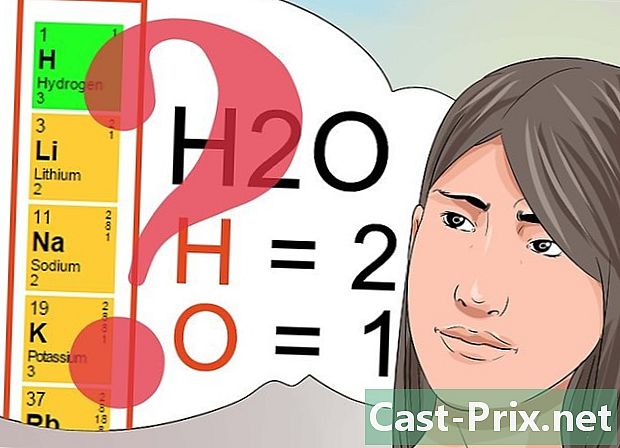
了解上标和下标中数字的含义。 如果您想通过考试,了解这些数字的含义很重要。- 上标中的数字遵循元素周期表中显示的模式,并指示化学元素或化合物的总电荷。重复元素周期表,您将看到沿着同一垂直列(组)排列的元素按指数共享相同的数字。
- 缩进数字用于确定被识别为化合物一部分的每种元素的量。如上所述,分子H 2 O的指数2表示存在两个氢原子。
-

发现原子之间如何反应。 化学中使用的部分术语包括有关某些类型反应产生的产物命名的特定规则。- 这些反应之一是氧化还原反应。这是获取或丢失电子的反应。
- 要记住在氧化还原反应过程中发生的机理,请记住该名称 RROO。这是记住这一点的简单方法 氧化剂获取时还原剂产生电子.
-
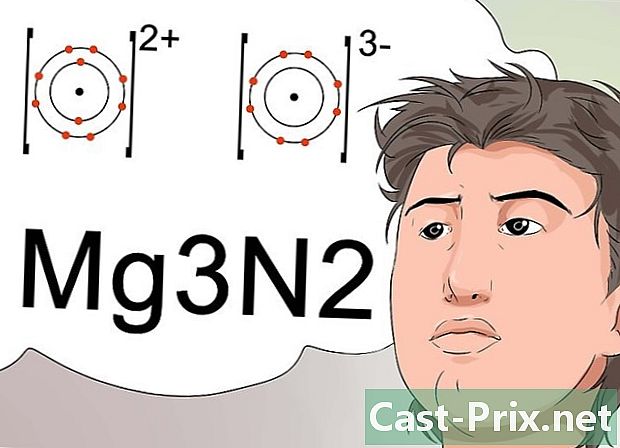
使用线索中的数字获得中性分子。 科学家利用线索来确定化合物的确定分子式,这也表明该化合物在带中性电荷的情况下是稳定的。- 为了获得稳定的电子配置,必须用等强度的负离子(阴离子)对正离子(阳离子)进行补偿。参展商代表了负载。
- 例如,狮子镁带有+2的正电荷,而狮子氮带有-3的负电荷。数字+2和-3应该放在上标中。为了使两种元素适当地结合以获得中性分子,必须将3个镁原子用于2个氮原子。
- 因此,获得的分子是Mg3N2。
-
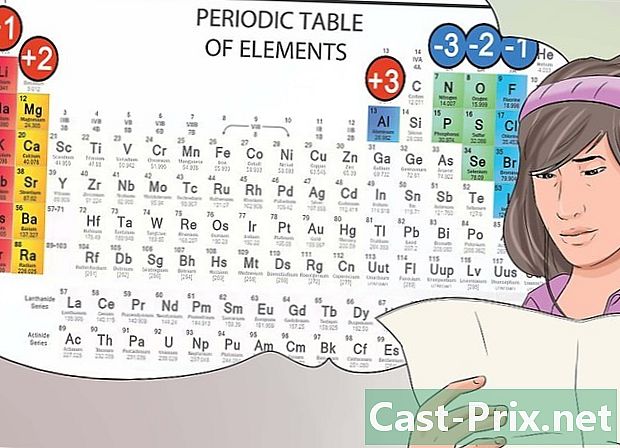
从其位置识别阴离子和阳离子。 在元素周期表中,属于第一组的元素被视为碱金属,并且具有+1的正电荷。钠(Na +)和锂(Li +)是示例。- 碱土金属是第二族的一部分,并形成2+阳离子,例如镁(Mg2 +)和钡(Ba2 +)。
- 属于元素周期表第七列的化学元素构成卤素族,并形成带有负电荷的阴离子,例如氯(Cl-)和锂(I-)。
-

识别最常见的阳离子和阴离子。 要在化学考试中取得成功,您将必须尽可能多地了解其元素的指数没有变化的命名法。- 换句话说,镁始终以Mg表示,并始终具有+2正电荷。
-

尽量不要让信息淹没自己。 不容易理解和记住有关元素或化合物的不同化学反应,电子交换和电荷变化的所有详细信息。- 用描述性术语表达您不理解的主题。例如,如果您不了解氧化反应或元素如何与负电荷和正电荷结合,请这样说。通过清楚表达对您有问题的概念,您可能会注意到您对事物有很多控制权。
-

定期与您的老师见面。 创建您不了解的主题列表,并请教您的老师。这是一个吸收复杂概念的机会,然后再输入更复杂和难以理解的课堂概念。 -

告诉自己您正在学习一种新语言。 理解写来指示电荷,分子中的硅藻原子数以及分子之间形成的键的化学式是化学语言的一部分。这是一种以图形方式表示并以书面形式表示化学反应期间发生的不同转化的方式,而我们看不到。- 如果所有的机理都可以用肉眼观察到,那么对化学的理解就会容易得多。但是,您必须努力理解化学中用于描述现象以及反应机理的术语。
- 如果您在理解化学课方面有困难,请知道您并不孤单。但是,不要上当。与您的老师交谈,分组学习,联系您的老师的助手或向真正擅长化学的人寻求帮助。您可以学习整个课程,但最好寻求帮助,以便我们向您解释以更好地理解某些章节。